當(dāng)前位置:美谷分子儀器(上海)有限公司>>技術(shù)文章>>【前沿?zé)狳c(diǎn)】石榴的腸道菌群代謝產(chǎn)物可提高免疫系統(tǒng)抗癌能力
【前沿?zé)狳c(diǎn)】石榴的腸道菌群代謝產(chǎn)物可提高免疫系統(tǒng)抗癌能力
UA以T細(xì)胞依賴性的方式抑制腸腫瘤生長(zhǎng)
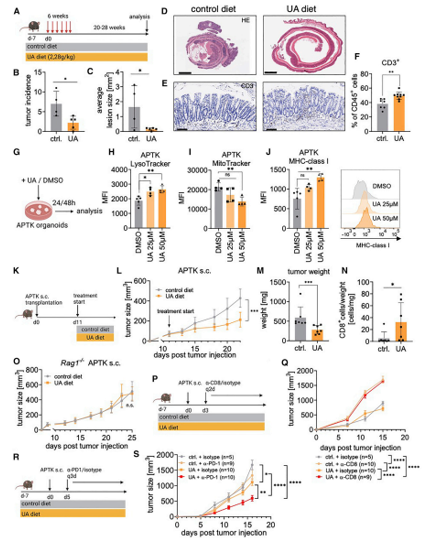
為了研究UA依賴性自噬是否模仿了Stat3△IEC小鼠的效果,并以T細(xì)胞依賴性的方式阻止了腸道腫瘤的發(fā)展,研究者們采用了氧化偶氮甲烷 (AOM)誘導(dǎo)的腫瘤發(fā)生模型。FVB小鼠每周注射一次致癌物AOM,持續(xù)6周,并以含UA的飼料(2.28 g/kg)或?qū)φ诊暳衔桂B(yǎng)18周(圖1A)。口服UA可顯著降低腫瘤發(fā)生率和腫瘤大小(圖1B-1D)。隨之而來(lái)的是CD3+ T細(xì)胞浸潤(rùn)到結(jié)腸黏膜的增多(圖1E和1F)。結(jié)合腫瘤類器官APTK 類器官 (characterized by loss of Apc, Trp53, and Tgfbr2 as well as expression of oncogenic KrasG12D)系統(tǒng)實(shí)驗(yàn) ,證實(shí)了UA誘導(dǎo)的腫瘤抑制依賴于T細(xì)胞。
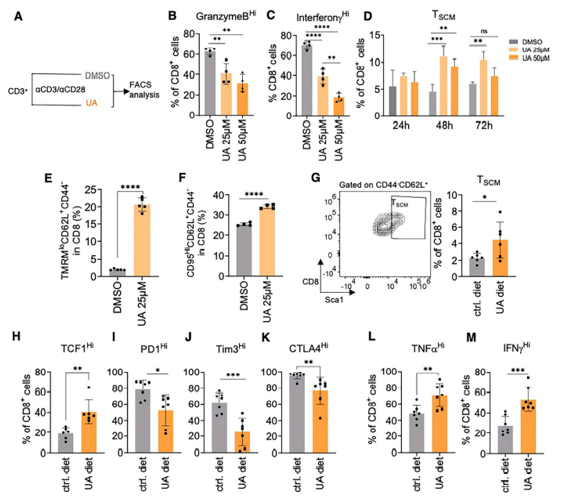
線粒體重塑與T細(xì)胞命運(yùn)的改變有關(guān)。考慮到UA效應(yīng)對(duì)CD8+ T細(xì)胞的依賴性,研究者們想了解UA是否也可能直接影響T細(xì)胞的命運(yùn)。從FVB小鼠中純化的T細(xì)胞被αCD3/αCD28珠刺激,誘導(dǎo)T細(xì)胞分化為效應(yīng)T細(xì)胞亞群,無(wú)論UA存在與否,持續(xù)72小時(shí)。UA給藥阻斷了向效應(yīng)T細(xì)胞的分化(圖2B和2C),并導(dǎo)致幼稚CD44loCD62Lhi T細(xì)胞顯著增加。此外,還觀察到中樞記憶細(xì)胞(TCM)的減少,而效應(yīng)記憶細(xì)胞(TEM)的頻率保持不變。在CD4+細(xì)胞中,只觀察到較晚時(shí)間點(diǎn)的變化,其特征是CD4+細(xì)胞的幼稚樣減少,但TEM細(xì)胞的頻率增強(qiáng)。
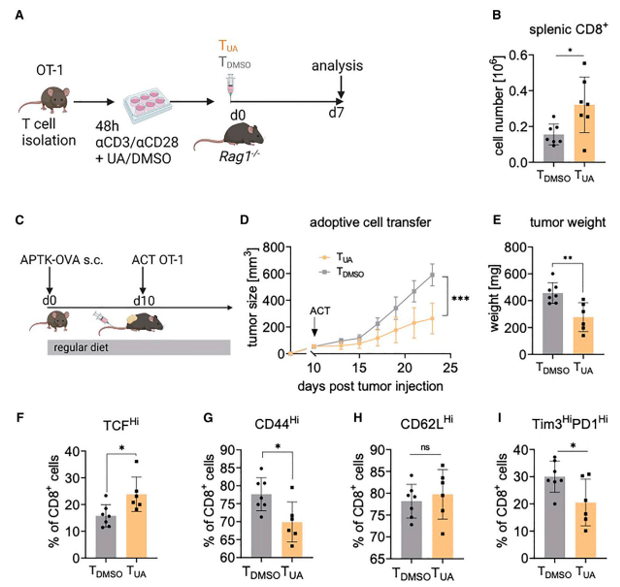
研究者們進(jìn)一步證實(shí),在給CD8+ T細(xì)胞服用UA后6小時(shí)內(nèi),線粒體膜電位降低(圖4A和4B)。這伴隨著增強(qiáng)的溶酶體形成(圖4C), 24小時(shí)后,線粒體含量以劑量依賴性的方式丟失(圖4D)。后者可以在所有分析的T細(xì)胞亞群中檢測(cè)到,因此提示有絲分裂的誘導(dǎo)。圖4的其他數(shù)據(jù)也有力地支持了UA誘導(dǎo)的依賴于Pink1的自噬觸發(fā)TSCM的形成以增強(qiáng)抗腫瘤免疫的觀點(diǎn)。
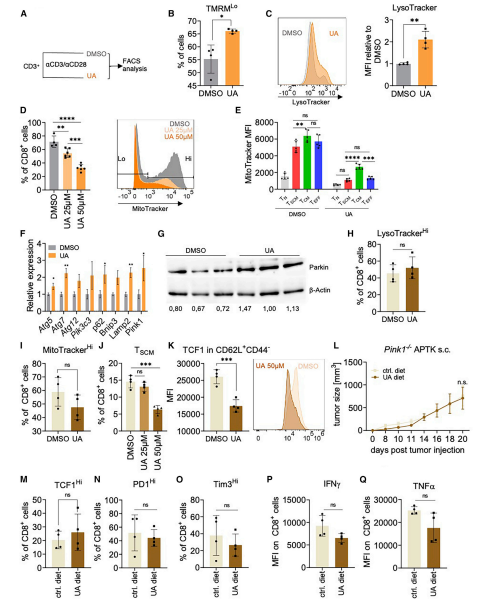
圖4
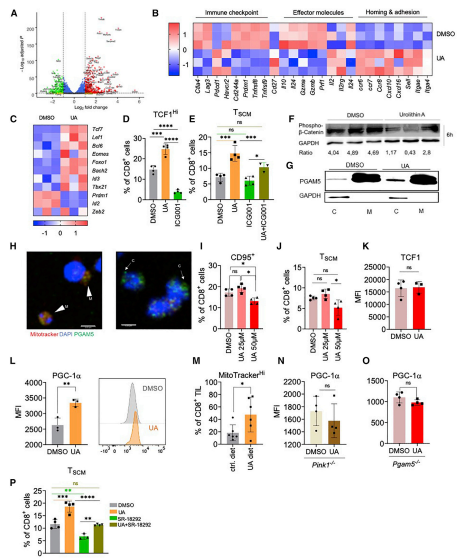
圖5
最后,研究者們希望確定UA是否會(huì)導(dǎo)致人類CD8+ T細(xì)胞中TSCM細(xì)胞的擴(kuò)增。從健康獻(xiàn)血者的外周血單個(gè)核細(xì)胞(PBMCs)中分離出人CD3+ T細(xì)胞,并在UA存在的情況下體外用αCD3/αCD28珠刺激它們。事實(shí)上,在5 / 5個(gè)人供體中,UA增加了基于CD45RA+CCR7HiCD62L+CD95+CD8+表達(dá)的人類TSCM細(xì)胞的頻率(圖6B;圖S5A和S5B)。與小鼠T細(xì)胞一樣,UA處理48小時(shí)后,人CD8+ T細(xì)胞顯示出線粒體膜電位下降(圖6C),細(xì)胞內(nèi)染色證實(shí)TCF1表達(dá)增加(圖6D),證實(shí)UA誘導(dǎo)小鼠和人T細(xì)胞的記憶干細(xì)胞特征。為了確定UA引發(fā)的自噬是否也構(gòu)成了誘導(dǎo)CAR-TSCM的可行策略,在存在或不存在UA的情況下,激活的T細(xì)胞通過(guò)慢病毒載體(VSV-LV)轉(zhuǎn)導(dǎo)CD19-CAR基因。轉(zhuǎn)導(dǎo)后3天,測(cè)定CAR -表達(dá)TSCM的數(shù)量(圖6E)。UA不影響基因傳遞到CD8+細(xì)胞;然而,盡管在UA暴露后,CAR-表達(dá)的TSCM細(xì)胞顯著增加,約占CD8+細(xì)胞的60%(圖6F),但這對(duì)CD19 CAR- T細(xì)胞介導(dǎo)的NALM-6白血病細(xì)胞殺傷沒有負(fù)面影響(圖6G)。即使將UA應(yīng)用于先前冷凍的癌胚抗原特異性CAR - T細(xì)胞(CEA;圖6H),這種強(qiáng)烈增強(qiáng)的CAR - TSCM形成(圖6I)與表達(dá)CEA的人類CRC類器官的殺傷效果相當(dāng)(圖6J)。因此,UA顯著增強(qiáng)CAR-TSCM細(xì)胞的增殖。在CAR T 細(xì)胞殺傷實(shí)驗(yàn)中,采用了Molecular Devices 公司的SpectraMax iD3酶標(biāo)儀的發(fā)光模式進(jìn)行了數(shù)據(jù)讀取。
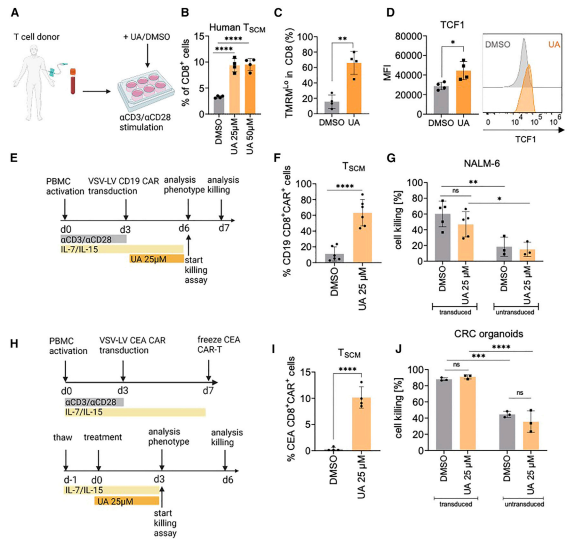
圖6
T記憶干細(xì)胞(TSCM)表現(xiàn)出增強(qiáng)的自我更新能力和延長(zhǎng)的生存能力,從而防止T細(xì)胞衰竭,促進(jìn)有效的抗腫瘤T細(xì)胞反應(yīng)。TSCM細(xì)胞可以被尿石素A (UA)擴(kuò)增。 (UA)是由腸道微生物群系從富含鞣花丹寧的食物中產(chǎn)生的,已被證明可以改善線粒體健康狀態(tài)。口服UA給荷瘤小鼠提供了強(qiáng)大的抗腫瘤CD8+ T細(xì)胞免疫,而體外UA預(yù)處理的T細(xì)胞在過(guò)繼細(xì)胞轉(zhuǎn)移后顯示出更好的抗腫瘤功能。UA誘導(dǎo)的TSCM的形成依賴于Pink1介導(dǎo)的自噬觸發(fā)線粒體磷酸酶Pgam5的胞質(zhì)釋放。胞質(zhì)Pgam5去磷酸化β-catenin,驅(qū)動(dòng)Wnt信號(hào)通路和代償性線粒體生物發(fā)生。總的來(lái)說(shuō),研究者們揭示了一個(gè)連接自噬和TSCM形成的關(guān)鍵信號(hào)通路,并認(rèn)為耐受性良好的代謝化合物UA是改善免疫治療的一個(gè)有吸引力的選擇。



會(huì)員.png) 8
8
