逆轉錄病毒簡介
病毒是一種由核酸分子和蛋白質構成的非細胞形態生物,能夠攜帶基因進入受體細胞,經開發和改造后可用作細胞基因治療(CGT)載體。通過改造后的病毒載體一般具有更好的安全性和更快的分子克隆速度,同時感染能力也得到了定向進化,從而具備了更快捷、更廣譜的轉導特性,以及更安全、更特異的感染特性。然而由于病毒的多樣性及宿主機體的高度復雜性,目前僅腺病毒、腺相關病毒、慢病毒、逆轉錄病毒和溶瘤病毒等少數種類可改造為CGT載體。
其中,逆轉錄病毒(Retrovirus)又稱反轉錄病毒,是一種RNA病毒,病毒顆粒為二十面體對稱結構、球形,有包膜,表面有刺突。逆轉錄病毒需在逆轉錄酶的作用下,將RNA轉變為cDNA,新合成的cDNA插入宿主的核DNA中,隨宿主DNA復制、轉錄、翻譯達到擴增目的。
按照目前國際病毒分類標準,逆轉錄病毒科分為7個屬:α逆轉錄病毒屬、β逆轉錄病毒屬、γ反轉錄病毒屬、δ反轉錄病毒屬、ε反轉錄病毒屬、慢病毒屬和泡沫病毒屬。在這些逆轉錄病毒中,僅γ-逆轉錄病毒和慢病毒用于臨床。
因此,通常所說的逆轉錄病毒載體是指在γ逆轉錄病毒(GRV)的基礎上改造獲得的,主要包括MMLV(莫洛尼氏鼠白血病逆轉錄病毒)和MSCV(鼠干細胞病毒)。這些載體能夠將外源基因有效地整合到宿主細胞的基因組中,實現長期穩定的基因表達。
γ-逆轉錄病毒載體具有簡單的基因組結構,由以下蛋白質編碼基因組成:gag、pol和env。Gag編碼衣殼蛋白,Pol編碼病毒酶(逆轉錄酶、整合酶和蛋白酶),Env編碼囊膜蛋白。

圖1. 基于小鼠白血病病毒(MLV)的γ逆轉錄病毒基因組的結構(doi:10.3390/v3060677)
γ-逆轉錄病毒載體包裝系統通常包括三個關鍵的質粒:包裝質粒(含有γ-逆轉錄病毒的gag、pol和rev基因)、載體質粒(包含目的基因、選擇標記基因以及必要的病毒序列)和包膜質粒(含病毒粒子的表面蛋白,如env基因)。
γ-逆轉錄病毒載體的生產平臺主要有兩種:一種是瞬時工藝,采用上述三質粒系統,共轉染到HEK293T包裝細胞系中,進行病毒制備;另外一種是穩定工藝,即以表達包裝和囊膜基因的包裝細胞系制備穩定產毒細胞株(如PG13)。
復制型逆轉錄病毒(RCR)概念及法規監管要求
通常,通過改造將逆轉錄病毒中與病毒包裝和轉導相關的基因刪除,替換為需要表達的外源基因,因此生產的病毒顆粒是復制缺陷型的,無法在細胞內復制并組裝為新的病毒顆粒,但能將外源基因整合到宿主基因組中持續表達。
目前制備CAR-T細胞所用的慢病毒和γ-逆轉錄病毒載體均為復制缺陷型,已極大降低了產生復制型病毒的風險,但病毒載體的制備方法以及制備過程中仍存在產生復制型慢病毒或復制型逆轉錄病毒的潛在風險。這些風險主要源自:病毒載體生產過程中,因穿梭質粒、包裝質粒及包裝細胞(eg.HEK293/HEK293T)中的內源性逆轉錄元件之間發生的同源或非同源重組;慢病毒載體與T細胞的內源性逆轉錄元件之間發生的同源或非同源重組。
因此,復制型病毒(RCV)可能在病毒載體生產階段、CAR-T細胞制備階段,甚至在患者接受治療后,隨著CAR-T細胞在體內的持續擴增,依然存在產生RCL/RCR的潛在風險。終產品中復制型病毒的存在有可能引起病人不良反應,構成臨床隱患和潛在危險,故對復制型病毒檢測是安全性檢測中非常重要的項目。
隨著病毒載體在CGT領域應用越來越廣泛,相關法規和技術原則對監測復制型病毒提出了建議。
國家藥品監督管理局藥品審評中心(CDE)在2020年9月發布《基因轉導與修飾系統藥學研究與評價技術指導原則(征求意見稿)》:采用復制缺陷型或條件復制型病毒載體時,應在生產工藝的適當階段檢測生產過程中可能產生的具有復制能力的病毒、親本病毒或野生型病毒進行檢測,并根據給藥劑量等確定殘留量的標準限度。常見的復制型病毒檢測方法包括指示細胞培養法、直接qPCR法等。可復制型逆轉錄病毒(RCR)檢測:建議采用敏感的指示細胞培養法進行RCR檢測。RCR擴增細胞與待測樣本進行共培養以大程度擴增RCR,在一定傳代次數和時間的傳代培養后取適量上清接種RCR指示細胞培養,以觀察、計數細胞病變集落或者進行RCR標志物的檢測。
2022年5月,CDE發布的《體外基因修飾系統藥學研究與評價技術指導原則(試行)》中提到RCR:


美國FDA 2020年發布的關于RCR/RCL檢測指南提出:對于RCR/RCL的檢測包含指示細胞培養法、ELISA法(p24蛋白測定)、PCR/Q-PCR法(通過psi-gag或VSV-G聚合酶鏈反應)、PERT法(產物增強性逆轉錄檢測法)共4種檢測方法。
復制型逆轉錄病毒(RCR)的檢測
中美歐三國監管機構對于復制型病毒的控制階段和檢測要求基本相同,在產品生產的各個階段以及在接受基于病毒載體的基因治療的患者后續監測中進行檢測。并且各監管機構推薦的復制型病毒的檢測方法均是指示細胞培養法,該方法是復制型病毒檢測的金標準。
但考慮到CAR-T細胞終產品一般需要新鮮輸注的特殊情況,基于細胞培養法的RCL/RCR檢測方法周期較長,建議在細胞產品制備過程中進行全面控制(如對慢病毒載體及生產終末細胞采用基于細胞培養方法測定RCL/RCR,以確保生產工藝過程中不存在RCL/RCR的風險),細胞終產品階段可采用qPCR快檢法快速放行。
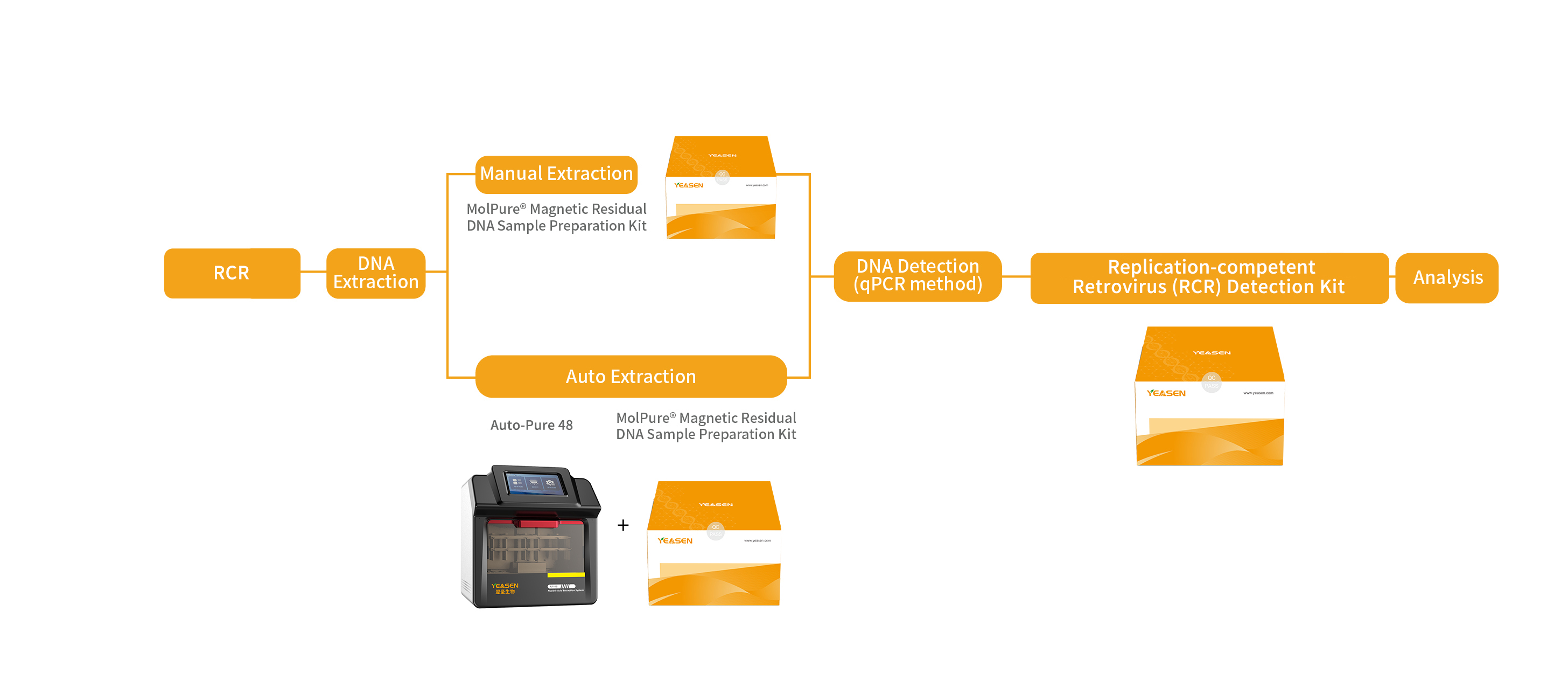
針對上述情況,翌圣生物自主研發了復制型逆轉錄病毒RCR檢測試劑盒,采用熒光探針RT-PCR法特異性擴增逆轉錄病毒載體上包含env在內的序列,專一快速的檢測各種使用逆轉錄病毒載體相關的細胞產品中可能發生的復制型逆轉錄病毒的潛在風險。還研發了與之配套使用的宿主細胞殘留DNA樣本前處理試劑盒,以及配套的自動化核酸提取儀器。
產品資質
符合法規:按照EP2.6.7、JP G3和USP 63藥典要求驗證,符合國際機構的標準;
配合審計:產品生產符合ISO13485質量體系標準,有完善的審計文件;
保障品質:試劑盒所需酶原料全自產,且已產業化,供貨穩定;
技術經驗積累:TaqMan法有技術沉淀,使得Kit靈敏度高;
專注產品性能:Taq酶抗體庫,雙封閉抗體提高了Kit特異性、穩定性等。
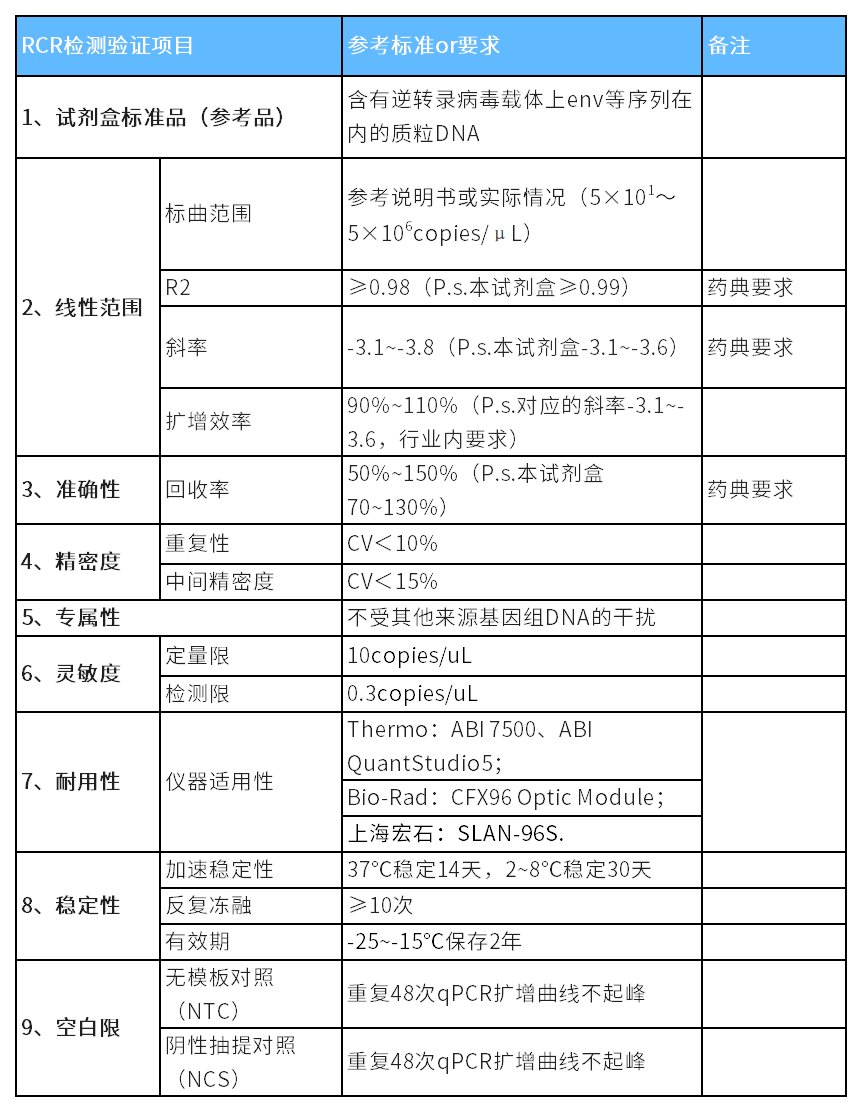
驗證內容
產品信息
產品 | 貨號 | 品名 | 規格 |
樣本前處理 試劑盒 | 18461ES | MolPure® Magnetic Residual DNA Sample Preparation Kit 磁珠法殘留DNA樣本前處理試劑盒(瓶裝) | 25T/100T |
18467ES | MolPure® Mag48 Sample Preparation Kit FN 磁珠法48孔樣本前處理試劑盒FN(預封裝) | 3×16T/ 6×16T | |
核酸提取儀器 | 80511ES | 48通道自動化核酸提取儀 | 48通量 |
RCR檢測試劑盒 | 41329ES | Replication-competent Lentivirus (RCR) Detection Kit 復制型逆轉錄病毒(RCR)檢測試劑盒 | 50T/100T |
相關產品
免責聲明
- 凡本網注明“來源:化工儀器網”的所有作品,均為浙江興旺寶明通網絡有限公司-化工儀器網合法擁有版權或有權使用的作品,未經本網授權不得轉載、摘編或利用其它方式使用上述作品。已經本網授權使用作品的,應在授權范圍內使用,并注明“來源:化工儀器網”。違反上述聲明者,本網將追究其相關法律責任。
- 本網轉載并注明自其他來源(非化工儀器網)的作品,目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責,不承擔此類作品侵權行為的直接責任及連帶責任。其他媒體、網站或個人從本網轉載時,必須保留本網注明的作品第一來源,并自負版權等法律責任。
- 如涉及作品內容、版權等問題,請在作品發表之日起一周內與本網聯系,否則視為放棄相關權利。
 手機版
手機版 化工儀器網手機版
化工儀器網手機版
 化工儀器網小程序
化工儀器網小程序
 官方微信
官方微信 公眾號:chem17
公眾號:chem17
 掃碼關注視頻號
掃碼關注視頻號




















 采購中心
采購中心