近幾十年的大量研究表明,在許多血液系統惡性腫瘤中,微小殘留病灶(MRD)與臨床結果及預后顯著相關。癌癥中MRD是指癌癥治療達到*緩解后,用常規的形態學檢測方法不能檢測到明顯的癌病灶,而此時體內仍存在的少量癌細胞。微小殘留病灶是腫瘤復發的直接原因。
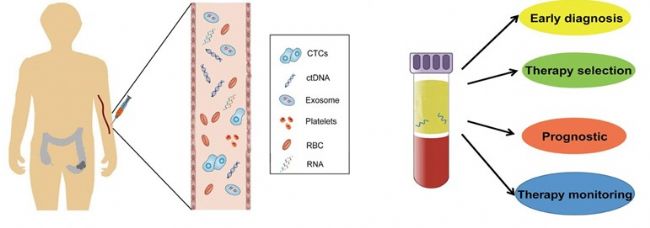
目前應用廣泛精確的MRD檢測手段是通過取患者的血液,對其中的循環腫瘤DNA(ctDNA)進行檢測,這種方法也叫做液體活檢(liquid biopsy),它可以獲取患者腫瘤病變信息,用以幫助診斷治療。
臨床研究主要是基于聚合酶鏈反應(PCR)的方法對淋巴疾病的MRD進行評估。一篇描述PCR在淋巴瘤MRD檢測中的臨床研究由Gribben JG在1991年發表。隨后又引入了基于TaqMan的實時PCR(qPCR),它可以定量分子靶標。目前,qPCR是用于MRD檢測的標準化方法,但該方法有一定的局限性,由于MRD本身的特征,常規的qPCR在檢測時往往達不到理想的效果。
為了克服標準分子技術的一些缺陷,需要高精度、高通量的MRD檢測工具,數字PCR技術作為第三代PCR技術,在靈敏度以及準確性度上遠遠優于qPCR。如一篇文章中報道,研究人員利用數字PCR以及二代測序技術對淋巴增生性疾病MRD進行監測,探究其在液體活檢方面的可行性。

在本篇文章中,研究人員發現與qPCR相比,數字PCR在進行MRD研究中具有許多實用優勢。數字PCR無需依靠標準曲線進行樣品定量,可以避免因反應效率波動而導致的結果差異,使那些由于診斷時腫瘤負荷低而無法生成可靠的標準曲線的患者得以康復。而且,它可以幫助節省寶貴診斷時間。
此外,文章報道了數字PCR技術在其他惡性血液病的MRD評價方面取得了較大進展。例如,在慢性髓系白血病中,與標準qPCR相比,數字PCR在低轉錄水平樣本的檢測上更加準確。
本研究表明,數字PCR可能會改變當前的MRD監測方法,從而使將來的試驗可以更好地表征血液系統疾病,幫助研究人員開發出MRD檢測的個性化方法。法國Stilla Technologies的Naica微滴芯片式數字PCR系統,利用cutting-edge微流體創新型芯片—Sapphire芯片作為數字PCR過程的耗材。樣品通過毛細通道網格以30,000個微滴的形式進入2D芯片中。并且還是3色熒光檢測儀器,整個流程只需要兩個半小時。結合強大的圖像分析技術和直觀可視的檢測功能,從而達到了數字PCR定量的置信水平,獲得的數據真實可信。

三通道檢測:兼容FAM, Evagreen /Cy3, VIC, HEX,/Cy5, Quasar® 705等染料,三色熒光檢測,快速建立多重實驗

微滴回溯:精確到單個微滴圖像

簡單操作,快速方便,全程只需兩個半小時

如果您想了解更多產品信息
請輸入賬號
請輸入密碼
請輸驗證碼
以上信息由企業自行提供,信息內容的真實性、準確性和合法性由相關企業負責,化工儀器網對此不承擔任何保證責任。
溫馨提示:為規避購買風險,建議您在購買產品前務必確認供應商資質及產品質量。